Canais especiais
Últimas matérias
Publicidade
Assuntos em alta
Saúde geral
Exames
Doenças populares

Dengue
No Brasil, os vírus da doença são transmitidos pela fêmea do mosquito Aedes aegypti. Conheça os sintomas da dengue e como se prevenir.
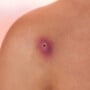
Furúnculo
O furúnculo é a inflamação de folículos capilares, geralmente do tamanho de uma ervilha, que atinge regiões como virilha e axila.

Infecção urinária
A infecção urinária pode afetar a bexiga (cistite) e rins. Conheça as causas e tratamentos caseiros para tratar a infecção urinária.
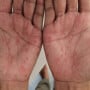
Sífilis
Sífilis é uma infecção sexualmente transmissível que causa sintomas como feridas e vermelhidão na pele. Veja os estágios e fotos da sífilis.
HIV
HIV é o vírus da imunodeficiência humana, uma infecção sexualmente transmissível, e o causador da aids. Conheça o teste, sintomas e causas para o HIV.

Urticária
A urticária pode ter diferentes causas, como alergia e estresse. Entenda todos os tipos e como tratar e aliviar o incômodo.
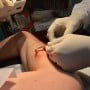
Berne
Berne é uma infecção parasitária causada por larvas da mosca-varejeira na pele, com foco na cabeça, pernas e braços. Veja como tirar berne e fotos.
Tratamentos populares

Proteína C-reativa
Exame mede a dosagem de PCR que pode indicar processos inflamatórios e infecciosos. Veja o que pode ser quando a proteína C-reativa está alta ou baixa
Oxandrolona
Oxandrolona é comumente usado para o ganho de massa muscular, porém não é indicado para essa finalidade. Conheça os efeitos colaterais e riscos

Laqueadura
Laqueadura é a ligação ou corte das trompas para prevenir uma possível gravidez. Entenda como funciona, para quem é indicado, cuidados.

injeção anticoncepcional
Injeção anticoncepcional é um método contraceptivo aplicado mensal ou trimestralmente para evitar a gravidez. Veja como tomar, tipos, prós e contras.

Remédio para emagrecer
Remédios para emagrecer são considerados uma forma simples de perder peso. Veja os principais remédios para emagrecer e como eles agem no organismo.

Carvão ativado
O carvão ativado não é o mesmo utilizado para churrasco. Entenda quais são os benefícios, como usar e onde comprar o carvão ativado

Reiki
O reiki é uma terapia integrativa que proporciona benefícios físicos e mentais através da canalização de energia. Entenda para que serve o reiki.

Barras de Access
Método promete tratar questões emocionais a partir de toques na cabeça. Entenda quais são os pontos das barras de access e se realmente funciona.
Medicamentos populares

Beta Trinta: para que serve e como usar
Laboratório: EMS
BetaTrinta é indicado para o tratamento de doenças agudas e crônicas...

Ibuprofeno: para que serve e como usar
Medicamento Genérico.
Laboratório: Prati Donaduzzi
Este medicamento tem ação contra a inflamação (reação de defesa do...
Diprospan: para que serve e como usar
Laboratório: Mantecorp
DIPROSPAN® está indicado para o tratamento de doenças agudas e...

Acetato de dexametasona: para que serve e como usar
Medicamento Genérico.
Laboratório: Multilab
Este medicamento é destinado ao tratamento de doenças inflamatórias...

Fosfato sódico de prednisolona: para que serve e como tomar?
Medicamento Genérico.
Laboratório: Cimed
O fosfato sódico de prednisolona é indicado como agente...

Toragesic: para que serve, composição e como tomar?
Laboratório: EMS
Toragesic® é um anti-inflamatório não hormonal, de potente ação...

Decadron: para que serve e como usar
Laboratório: Aché
DECADRON comprimidos/elixir é indicado no tratamento de sintomas de...

Rivotril: para que serve e como usar
Laboratório: Roche
Distúrbio epiléptico Rivotril® é indicado para tratar crises...
Publicidade
Publicidade
Matérias mais populares
Respostas de especialistas mais lidas

1 Pessoa perguntou
Como tratar colesterol quando se tem hipotireoidismo e mais de 35 anos?
[ Continuar lendo ]
Dr. Bruno Valdigem
Cardiologia
CRM 118535/SP
1 Pessoa perguntou
Colesterol total e triglicérides elevados podem ser resolvidos com dieta e exercícios na adolescência?
[ Continuar lendo ]
Dr. Bruno Valdigem
Cardiologia
CRM 118535/SP

Dr. Bruno Valdigem
Cardiologia
CRM 118535/SP
1 Pessoa perguntou
Colesterol alto pode ser revertido só com dieta e exercícios ou eu preciso tomar medicamentos?
[ Continuar lendo ]
Dr. Bruno Valdigem
Cardiologia
CRM 118535/SP
1 Pessoa perguntou
Colesterol alto pode causar aumento nas taxas de ácido úrico?
[ Continuar lendo ]
Dr. Bruno Valdigem
Cardiologia
CRM 118535/SP


1 Pessoa perguntou
Uma vez com colesterol alto, é possível remover as gorduras já aderidas aos vasos sanguíneos?
[ Continuar lendo ]
Dr. Roberto Navarro
Nutrologia
CRM 78392/SP
Nossos especialistas mais consultados